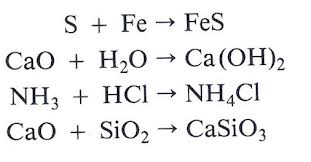Reacciones Químicas
7.1 Simbolos para la escritura de ecuaciones quimicas
7.2 Reacciones de síntesis, descomposición, sustitución simple y sustitución doble
Reacción de síntesis
Existen diferentes tipos de reacciones químicas. Una reacción de síntesis es aquella que lleva a que dos sustancias distintas (es decir, dos reactivos) se combinen para dar lugar a un único producto. Puede decirse, por lo tanto, que dos elementos sencillos, a través de una reacción de síntesis, se unen y crean un compuesto complejo.
Reacción de síntesis
Existen diferentes tipos de reacciones químicas. Una reacción de síntesis es aquella que lleva a que dos sustancias distintas (es decir, dos reactivos) se combinen para dar lugar a un único producto. Puede decirse, por lo tanto, que dos elementos sencillos, a través de una reacción de síntesis, se unen y crean un compuesto complejo.
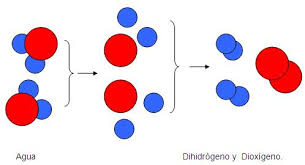
Reacciones de descomposición
Una reacción de descomposición consiste en separar los distintos constituyentes de un compuesto hasta alcanzar el número de elementos que lo forman de manera independiente.
Las mezclas son cuerpos de dos o más sustancias puras (elementos o compuestos), que pueden separarse por procedimientos físicos.
Las reacciones de descomposición se verifican, por lo general, con presencia de calor y en ellas un compuesto puede producir:
Una reacción de descomposición consiste en separar los distintos constituyentes de un compuesto hasta alcanzar el número de elementos que lo forman de manera independiente.
Las mezclas son cuerpos de dos o más sustancias puras (elementos o compuestos), que pueden separarse por procedimientos físicos.
Las reacciones de descomposición se verifican, por lo general, con presencia de calor y en ellas un compuesto puede producir:
- Dos elementos.
- Dos o más compuestos.
- Uno o más compuestos y uno o más elementos.
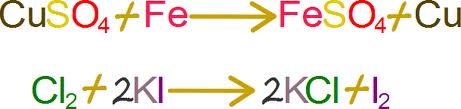
Reacciones de simple sustitución:
Denominadas también de simple desplazamiento cuando una sustancia simple reacciona con otra compuesta, reemplazando a uno de sus componentes.
Sustitución simple. Se forma por intercambio de iones entre dos compuestos
Cu + Ag NO3 Cu NO3 + Ag
El cobre sustituye la plata
Denominadas también de simple desplazamiento cuando una sustancia simple reacciona con otra compuesta, reemplazando a uno de sus componentes.
Sustitución simple. Se forma por intercambio de iones entre dos compuestos
Cu + Ag NO3 Cu NO3 + Ag
El cobre sustituye la plata
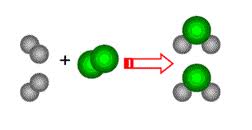
Reacción sustitución doble
También se denomina de doble desplazamiento y ocurre cundo hay un intercambio de elementos entre los dos compuestos diferentes y de esta manera originan nuevas sustancias.
se presenta cuando la sustancias reaccionantes estan en estado ionoco por encontrars en solucion, combinandos entre si sus iones con mucha facilidad para formar sustancia que permanecen estables en el medio reaccionante
También se denomina de doble desplazamiento y ocurre cundo hay un intercambio de elementos entre los dos compuestos diferentes y de esta manera originan nuevas sustancias.
se presenta cuando la sustancias reaccionantes estan en estado ionoco por encontrars en solucion, combinandos entre si sus iones con mucha facilidad para formar sustancia que permanecen estables en el medio reaccionante
7.3 Métodos de balanceo de ecuaciones químicas por tanteo y por oxido-reducción
Cuando la reacción química se expresa como ecuación, además de escribir correctamente todas las especies participantes (nomenclatura), se debe ajustar el número de átomos de reactivos y productos, colocando un coeficiente a la izquierda de los reactivos o de los productos
Tanteo
Consiste en dar coeficientes al azar hasta igualar todas las especies.
Ejemplo:
CaF2 + H2SO4 ® CaSO4 + HF
Ecuación no balanceada
El número de F y de H esta des balanceado, por lo que se asignará (al azar) un coeficiente en la especie del flúor de la derecha.
CaF2 + H2SO4 ® CaSO4 + 2 HF
Oxidación y Reducción
Oxidación
La oxidación ocurre cuando una especie química pierde electrones y al mismo tiempo, aumenta su número de oxidación. Por ejemplo, el Sodio metálico (con número de oxidación cero), se puede convertir en el ion sodio (con carga de 1+) por la pérdida de dos electrones, según el esquema simbólico siguiente:
Na(0) ---> Na (1+) + 1e-
Reducción
La reducción ocurre cuando una especie química gana electrones y simultáneamente disminuye su número de oxidación. Por ejemplo, el cloro atómico (con número de oxidación cero) se convierte en el ion cloruro
(con número de oxidación y carga de 1–) por ganancia de un electrón, según el esquema simbólico siguiente:
1e- + Cl (0) ----> Cl (1-)
Cuando la reacción química se expresa como ecuación, además de escribir correctamente todas las especies participantes (nomenclatura), se debe ajustar el número de átomos de reactivos y productos, colocando un coeficiente a la izquierda de los reactivos o de los productos
Tanteo
Consiste en dar coeficientes al azar hasta igualar todas las especies.
Ejemplo:
CaF2 + H2SO4 ® CaSO4 + HF
Ecuación no balanceada
El número de F y de H esta des balanceado, por lo que se asignará (al azar) un coeficiente en la especie del flúor de la derecha.
CaF2 + H2SO4 ® CaSO4 + 2 HF
Oxidación y Reducción
Oxidación
La oxidación ocurre cuando una especie química pierde electrones y al mismo tiempo, aumenta su número de oxidación. Por ejemplo, el Sodio metálico (con número de oxidación cero), se puede convertir en el ion sodio (con carga de 1+) por la pérdida de dos electrones, según el esquema simbólico siguiente:
Na(0) ---> Na (1+) + 1e-
Reducción
La reducción ocurre cuando una especie química gana electrones y simultáneamente disminuye su número de oxidación. Por ejemplo, el cloro atómico (con número de oxidación cero) se convierte en el ion cloruro
(con número de oxidación y carga de 1–) por ganancia de un electrón, según el esquema simbólico siguiente:
1e- + Cl (0) ----> Cl (1-)