Enlaces Químicos e Interacciones Intermoleculares
5.1 Enlace Químico
Un enlace químico es la fuerza que existe entre dos o más
átomos, esta fuerza es justamente lo que mantiene unidos a ambos átomos para
formar las moléculas, pero es importante saber que, para enlazarse entre sí, los
átomos deben ceder, aceptar o compartir electrones.
Son justamente los electrones de valencia los que
determinarán el tipo de enlace químico que unirá a la molécula,
es decir que, según los electrones de valencia podremos saber a grandes rasgos
de que forma se unirá un átomo a otro, y qué características
tendrá dicho enlace.
Un enlace químico es la fuerza que existe entre dos o más
átomos, esta fuerza es justamente lo que mantiene unidos a ambos átomos para
formar las moléculas, pero es importante saber que, para enlazarse entre sí, los
átomos deben ceder, aceptar o compartir electrones.
Son justamente los electrones de valencia los que
determinarán el tipo de enlace químico que unirá a la molécula,
es decir que, según los electrones de valencia podremos saber a grandes rasgos
de que forma se unirá un átomo a otro, y qué características
tendrá dicho enlace.
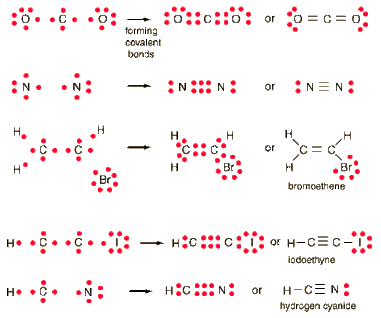
5.2 Regla del octeto
Esta regla indica que cuando se van a enlazar dos átomos iguales, los electrones de valencia
de éstos se organizan de tal manera que, al formar el enlace por
compartición de pares de electrones, cada uno de los átomos al final adopta una
estructura de gas noble, quedando ambos rodeados de 8 electrones en sus
últimos niveles de energía. Cuando se trata de átomos diferentes, el
elemento más electronegativo o no metálico es el que se rodea de ocho
electrones.
Esta Regla tiene algunos excepciones como es el caso de que no se aplica en la formación de
enlaces con pares de átomos de hidrógeno.
Aplicación de la regla dl octeto con átomos de elementos diferentes:
Esta regla indica que cuando se van a enlazar dos átomos iguales, los electrones de valencia
de éstos se organizan de tal manera que, al formar el enlace por
compartición de pares de electrones, cada uno de los átomos al final adopta una
estructura de gas noble, quedando ambos rodeados de 8 electrones en sus
últimos niveles de energía. Cuando se trata de átomos diferentes, el
elemento más electronegativo o no metálico es el que se rodea de ocho
electrones.
Esta Regla tiene algunos excepciones como es el caso de que no se aplica en la formación de
enlaces con pares de átomos de hidrógeno.
Aplicación de la regla dl octeto con átomos de elementos diferentes:
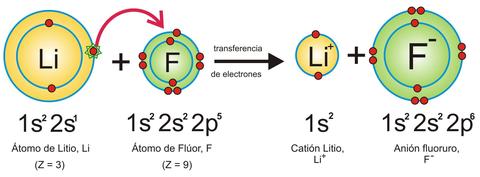
5.3 Enlace iónico y sus propiedades
Los compuestos iónicos suelen ser frecuentemente sólidos cristalinos que presentan
diferentes formas de cristalización. Una vez que se han formado los iones, positivos y negativos,
interaccionan electrostáticamente y como estas fuerzas electrostáticas son radiales, es decir,
no tienen una dirección determinada, cada ion tiende a rodearse del mayor número posible de
iones de signo contrario.
Sin embargo, hay una limitación que viene dada por el tamaño relativo de los cationes y
de los iones. Y otra limitación que viene dada por el número de cargas del catión y del anión,
ya que el cristal iónico en su conjunto tiene que ser electroneutro.
Propiedades delos compuestos con enlace iónico:
Los compuestos iónicos suelen ser frecuentemente sólidos cristalinos que presentan
diferentes formas de cristalización. Una vez que se han formado los iones, positivos y negativos,
interaccionan electrostáticamente y como estas fuerzas electrostáticas son radiales, es decir,
no tienen una dirección determinada, cada ion tiende a rodearse del mayor número posible de
iones de signo contrario.
Sin embargo, hay una limitación que viene dada por el tamaño relativo de los cationes y
de los iones. Y otra limitación que viene dada por el número de cargas del catión y del anión,
ya que el cristal iónico en su conjunto tiene que ser electroneutro.
Propiedades delos compuestos con enlace iónico:
- El enlace iónico es fuerte, las Uret son muy exotérmicas, lo que implica
que cuesta mucha energía romper la estructura cristalina al fundir.
Es decir, tendrán puntos de fusión altos. - Los cristales iónicos son duros, porque el enlace es fuerte y se resisten
bastante a ser rayados. - Sin embargo, son frágiles. Esto es debido a que un golpe puede
originar un desplazamiento de los planos de los iones y, al dejar
enfrentados iones de igual signo, daría lugar a una fractura en el cristal por
fuerzas repulsivas electrostáticas. - No conducen la corriente eléctrica en estado sólido porque los iones están
inmovilizados en la red; pero, al disolverse o fundirse estos iones adquieren
movilidad y pueden conducir la corriente eléctrica. - Se disuelven en disolventes polares, porque los dipolos de estos disolventes
rodean a los iones de la red cristalina y los van "arrancando" de la red.
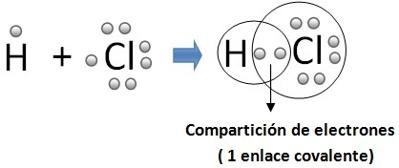
5.4 Enlace covalente
Los enlaces covalentes se definen como la unión
que se produce entre 2 átomos por la
compartición de 2 o más electrones de su capa externa con objeto de formar una
molécula estable.
Dentro de los enlaces covalentes nos encontramos con 2 tipos de enlaces covalentes
que se pueden originar:
Se origina cuando uno de los átomos dispone de mayor fuerza de atracción de los electrones
hacia su núcleo, como resultado se origina una molécula con parte negativa y otra parte positiva (dipolo).
Los enlaces covalentes polares siempre se producen cuando el enlace se realiza entre 2 átomos diferentes.
El grado de polaridad de la molécula resultante del enlace covalente, depende de la fuerza o atracción
que atrae los electrones hacia un átomo, este concepto es definido mediante la electronegatividad.
Enlace covalente apolar
Se produce cuando ambos átomos disponen de la misma fuerza de atracción de los electrones
hacia su mismo núcleo.
Los enlaces covalentes apolares siempre se producen cuando el enlace se realiza entre 2
átomos iguales o con el mismo grado de electronegatividad.
El concepto de molécula o material polar o apolar es de suma importancia para el estudio
de los adhesivos, por lo general aquellas superficies que dispongan de moléculas o materiales
polares en su superficie serán óptimas para conseguir fácilmente un adhesivado duradero en el tiempo.
Los enlaces covalentes se definen como la unión
que se produce entre 2 átomos por la
compartición de 2 o más electrones de su capa externa con objeto de formar una
molécula estable.
Dentro de los enlaces covalentes nos encontramos con 2 tipos de enlaces covalentes
que se pueden originar:
- Enlace covalente polar
- Enlace covalente apolar
Se origina cuando uno de los átomos dispone de mayor fuerza de atracción de los electrones
hacia su núcleo, como resultado se origina una molécula con parte negativa y otra parte positiva (dipolo).
Los enlaces covalentes polares siempre se producen cuando el enlace se realiza entre 2 átomos diferentes.
El grado de polaridad de la molécula resultante del enlace covalente, depende de la fuerza o atracción
que atrae los electrones hacia un átomo, este concepto es definido mediante la electronegatividad.
Enlace covalente apolar
Se produce cuando ambos átomos disponen de la misma fuerza de atracción de los electrones
hacia su mismo núcleo.
Los enlaces covalentes apolares siempre se producen cuando el enlace se realiza entre 2
átomos iguales o con el mismo grado de electronegatividad.
El concepto de molécula o material polar o apolar es de suma importancia para el estudio
de los adhesivos, por lo general aquellas superficies que dispongan de moléculas o materiales
polares en su superficie serán óptimas para conseguir fácilmente un adhesivado duradero en el tiempo.
5.5 Características de los diferentes tipos de enlace covalente
Enlace covalente no polar
El hidrogeno es el primer elemento que presenta este
tipo de enlace, por ejemplo cuando dos átomos comparten sus electrones, ambos
adquieren la configuración del helio: 1s²
H + H --> H:H
Átomo de hidrogeno átomo de hidrogeno electrones compartidos
Se deduce entonces que un enlace covalente no polar, es aquel que se lleva acabo cuando
se unen dos átomos iguales; y por lo mismo con la misma electronegatividad.
Ejemplo: el enlace covalente en le F2 cada átomo de
flúor pose sus electrones propios y comparte otros dos, suficiente para
completar los ocho que tiene el neón en su ultimo nivel energético. Los
electrones más internos se omiten y solo se representa la compartición de los
externos y se simplifica cuando únicamente se representa el enlace compartido
por una línea de enlace.
Enlace covalente polar
El enlace covalente polar ocurre entre átomos diferentes. No existe una compartición
electrónica simétrica, dada la diferencia de electronegatividades existentes. Siempre hay
un átomo que es más electronegativo que otro y es el que atrae hacia si el par de electrones.
El enlace es mas polar cuanto mayor es la diferencia de electronegatividades entre los átomos
participantes.
Ejemplo: el florero de hidrogeno sus electronegatividades son 2.1 y 4.0, asi que si diferencia
es 1.9. La electronegatividad del flúor hace que atraiga hacia si el par de electrones.
Del lado del flúor hay más carga negativa (electrones), mientras que del lado del hidrogeno
hay mas carga positiva y se representa así:
H + F --> H:F
H – F
Enlace covalente no polar
El hidrogeno es el primer elemento que presenta este
tipo de enlace, por ejemplo cuando dos átomos comparten sus electrones, ambos
adquieren la configuración del helio: 1s²
H + H --> H:H
Átomo de hidrogeno átomo de hidrogeno electrones compartidos
Se deduce entonces que un enlace covalente no polar, es aquel que se lleva acabo cuando
se unen dos átomos iguales; y por lo mismo con la misma electronegatividad.
Ejemplo: el enlace covalente en le F2 cada átomo de
flúor pose sus electrones propios y comparte otros dos, suficiente para
completar los ocho que tiene el neón en su ultimo nivel energético. Los
electrones más internos se omiten y solo se representa la compartición de los
externos y se simplifica cuando únicamente se representa el enlace compartido
por una línea de enlace.
Enlace covalente polar
El enlace covalente polar ocurre entre átomos diferentes. No existe una compartición
electrónica simétrica, dada la diferencia de electronegatividades existentes. Siempre hay
un átomo que es más electronegativo que otro y es el que atrae hacia si el par de electrones.
El enlace es mas polar cuanto mayor es la diferencia de electronegatividades entre los átomos
participantes.
Ejemplo: el florero de hidrogeno sus electronegatividades son 2.1 y 4.0, asi que si diferencia
es 1.9. La electronegatividad del flúor hace que atraiga hacia si el par de electrones.
Del lado del flúor hay más carga negativa (electrones), mientras que del lado del hidrogeno
hay mas carga positiva y se representa así:
H + F --> H:F
H – F
5.6 Propiedades de los compuestos covalentes
Características:
Propiedades:
Características:
- Están formados por no metales + no metal.
- Forman moléculas verdaderas.
- Los no metales comparten electrones.
Propiedades:
- Pueden presentarse en estado líquido o gaseoso aunque también pueden ser sólidos,
Por lo tanto sus puntos de fusión y ebullición no son elevados. - Son solubles en solventes apolares.
- Son malos conductores del calor y la electricidad.
5.7 Teorías que explican el enlace metálico (teoría del mar de electrones la teoría de bandas)
Modelo de mar de electrones
Para explicar las propiedades características de los metales (su alta conductividad
eléctrica y térmica, ductilidad y maleabilidad, ...) se ha elaborado un modelo de enlace
metálico conocido como modelo de la nube o del mar de electrones:
Los elementos con un enlace metálico están compartiendo un gran número de electrones
de valencia, formando un mar de electrones rodeando un enrejado gigante de cationes.
Los metales tienen puntos de fusión más altos por lo que se deduce que hay enlaces más
fuertes entre los distintos átomos. La vinculación metálica es no polar, apenas hay
(para los metales elementales puros) o muy poco (para las aleaciones) diferencia de
electronegatividad entre los átomos que participan en la interacción de la vinculación, y
los electrones implicados en que es la interacción a través de la estructura cristalina del
metal. El enlace metálico explica muchas características físicas de metales, tales como fuerza,
maleabilidad, ductilidad, conducción del calor y de la electricidad, y lustre. La vinculación
metálica es la atracción electrostática entre los átomos del metal o los iones y electrones
des localizados. Esta es la razón por la cual se explica un deslizamiento de capas, dando por
resultado su característica maleabilidad y ductilidad. Los átomos del metal tienen por lo menos
un electrón de la valencia, no comparten estos electrones con los átomos vecinos, ni pierden
electrones para formar los iones. En lugar los niveles de energía externos de los átomos del metal
se traslapan. Son como enlaces covalentes.
Los átomos de los metales tienen pocos electrones en su última capa, por lo general
1, 2 ó 3. Éstos átomos pierden fácilmente esos electrones (electrones de valencia)
y se convierten en iones positivos, por ejemplo Na+, Cu2+, Mg2+. Los iones positivos
resultantes se ordenan en el espacio formando la red metálica. Los electrones de valencia
desprendidos de los átomos forman una nube de electrones que puede desplazarse a través de
toda la red. De este modo todo el conjunto de los iones positivos del metal queda unido mediante
la nube de electrones con carga negativa que los envuelve.
La teoría de bandas.
La teoría de bandas está basada en la mecánica cuántica y procede de la teoría de los orbitales
moleculares (TOM). En esta teoría, se considera el enlace metálico como un caso extremo del enlace
covalente, en el que los electrones de valencia son compartidos de forma conjunta y simultánea
por todos los cationes. Desaparecen los orbitales atómicos y se forman orbitales moleculares con
energías muy parecidas, tan próximas entre ellas que todos en conjunto ocupan lo que se franja de
denomina una “banda de energía”.
Aunque los electrones van llenando los orbitales moleculares en orden creciente de energía, estas
son tan próximas que pueden ocupar cualquier posición dentro de la banda.
La banda ocupada por los orbitales moleculares con los electrones de valencia se llama banda
de valencia, mientras que la banda formada por los orbitales moleculares vacíos se llama
banda de conducción. A veces, ambas bandas se solapan energéticamente hablando.
Este modelo explica bastante bien el comportamiento eléctrico no solo de las sustancias
conductoras sino también de las semiconductoras y las aislantes.
En los metales, sustancias conductoras, la banda de valencia se solapa energéticamente
con la banda de conducción que está vacía, disponiendo de orbitales moleculares vacíos que
pueden ocupar con un mínimo aporte de energía, es decir, que los electrones están casi libres
pudiendo conducir la corriente eléctrica.
En los semiconductores y en los aislantes, la banda de valencia no se solapa con la de conducción.
Hay una zona intermedia llamada banda prohibida.
En los semiconductores, como el Silicio o el Germanio, la anchura de la banda prohibida
no es muy grande y los electrones con suficiente energía cinética pueden pasar a la banda de
conducción, por esa razón, los semiconductores conducen la electricidad mejor en caliente.
Sin embargo, en los aislantes, la banda prohibida es tan ancha que ningún electrón puede saltarla.
La banda de conducción está siempre vacía.
Modelo de mar de electrones
Para explicar las propiedades características de los metales (su alta conductividad
eléctrica y térmica, ductilidad y maleabilidad, ...) se ha elaborado un modelo de enlace
metálico conocido como modelo de la nube o del mar de electrones:
Los elementos con un enlace metálico están compartiendo un gran número de electrones
de valencia, formando un mar de electrones rodeando un enrejado gigante de cationes.
Los metales tienen puntos de fusión más altos por lo que se deduce que hay enlaces más
fuertes entre los distintos átomos. La vinculación metálica es no polar, apenas hay
(para los metales elementales puros) o muy poco (para las aleaciones) diferencia de
electronegatividad entre los átomos que participan en la interacción de la vinculación, y
los electrones implicados en que es la interacción a través de la estructura cristalina del
metal. El enlace metálico explica muchas características físicas de metales, tales como fuerza,
maleabilidad, ductilidad, conducción del calor y de la electricidad, y lustre. La vinculación
metálica es la atracción electrostática entre los átomos del metal o los iones y electrones
des localizados. Esta es la razón por la cual se explica un deslizamiento de capas, dando por
resultado su característica maleabilidad y ductilidad. Los átomos del metal tienen por lo menos
un electrón de la valencia, no comparten estos electrones con los átomos vecinos, ni pierden
electrones para formar los iones. En lugar los niveles de energía externos de los átomos del metal
se traslapan. Son como enlaces covalentes.
Los átomos de los metales tienen pocos electrones en su última capa, por lo general
1, 2 ó 3. Éstos átomos pierden fácilmente esos electrones (electrones de valencia)
y se convierten en iones positivos, por ejemplo Na+, Cu2+, Mg2+. Los iones positivos
resultantes se ordenan en el espacio formando la red metálica. Los electrones de valencia
desprendidos de los átomos forman una nube de electrones que puede desplazarse a través de
toda la red. De este modo todo el conjunto de los iones positivos del metal queda unido mediante
la nube de electrones con carga negativa que los envuelve.
La teoría de bandas.
La teoría de bandas está basada en la mecánica cuántica y procede de la teoría de los orbitales
moleculares (TOM). En esta teoría, se considera el enlace metálico como un caso extremo del enlace
covalente, en el que los electrones de valencia son compartidos de forma conjunta y simultánea
por todos los cationes. Desaparecen los orbitales atómicos y se forman orbitales moleculares con
energías muy parecidas, tan próximas entre ellas que todos en conjunto ocupan lo que se franja de
denomina una “banda de energía”.
Aunque los electrones van llenando los orbitales moleculares en orden creciente de energía, estas
son tan próximas que pueden ocupar cualquier posición dentro de la banda.
La banda ocupada por los orbitales moleculares con los electrones de valencia se llama banda
de valencia, mientras que la banda formada por los orbitales moleculares vacíos se llama
banda de conducción. A veces, ambas bandas se solapan energéticamente hablando.
Este modelo explica bastante bien el comportamiento eléctrico no solo de las sustancias
conductoras sino también de las semiconductoras y las aislantes.
En los metales, sustancias conductoras, la banda de valencia se solapa energéticamente
con la banda de conducción que está vacía, disponiendo de orbitales moleculares vacíos que
pueden ocupar con un mínimo aporte de energía, es decir, que los electrones están casi libres
pudiendo conducir la corriente eléctrica.
En los semiconductores y en los aislantes, la banda de valencia no se solapa con la de conducción.
Hay una zona intermedia llamada banda prohibida.
En los semiconductores, como el Silicio o el Germanio, la anchura de la banda prohibida
no es muy grande y los electrones con suficiente energía cinética pueden pasar a la banda de
conducción, por esa razón, los semiconductores conducen la electricidad mejor en caliente.
Sin embargo, en los aislantes, la banda prohibida es tan ancha que ningún electrón puede saltarla.
La banda de conducción está siempre vacía.
5.8 Características que se derivan del enlace metálico
Características:
--Se da entre átomos metálicos.
--Los cationes forman una estructura cristalina y los electrones ocupan los intersticios
que quedan libres en ellos sin estar fijados en ningún catión concreto (mar de electrones)
--Los electrones están, pues, bastante libres pero estabilizan la estructura al tener carga contraria
a los cationes.
Propiedades:
--Suelen ser sólidos a temperatura ambiente.
--Tienen puntos de fusión y ebullición muy variado (aunque suelen ser más bien alto).
--Las conductividades térmicas y eléctricas son muy elevadas.
--Presentan brillo metálico.
--Son muy solubles en estado fundido en otros metales formando aleaciones.
--Son dúctiles y maleables (no frágiles).
Características:
--Se da entre átomos metálicos.
--Los cationes forman una estructura cristalina y los electrones ocupan los intersticios
que quedan libres en ellos sin estar fijados en ningún catión concreto (mar de electrones)
--Los electrones están, pues, bastante libres pero estabilizan la estructura al tener carga contraria
a los cationes.
Propiedades:
--Suelen ser sólidos a temperatura ambiente.
--Tienen puntos de fusión y ebullición muy variado (aunque suelen ser más bien alto).
--Las conductividades térmicas y eléctricas son muy elevadas.
--Presentan brillo metálico.
--Son muy solubles en estado fundido en otros metales formando aleaciones.
--Son dúctiles y maleables (no frágiles).
5.9 Fuerzas intermoleculares
Las fuerzas intermoleculares se definen como el conjunto de fuerzas atractivas y repulsivas
que se producen entre las moléculas como consecuencia de la presencia o ausencia de electrones.
Cuando dos o más átomos se unen mediante un enlace químico forman una molécula, los electrones
que conforman la nueva molécula recorren y se concentran en la zona del átomo con mayor
electronegatividad, definimos la electronegatividad como la propiedad que tienen los átomos
en atraer electrones.
La concentración de electrones en una zona específica de la molécula crea una carga negativa,
mientras que la ausencia de los electrones crea una carga positiva.
Denominamos dipolos a las moléculas que disponen de zonas cargadas negativamente y
positivamente debido a la electronegatividad y concentración de los electrones en las moléculas.
Podemos asimilar el funcionamiento de un dipolo a un imán con su polo positivo y su polo negativo,
de tal forma que si acercamos otro imán el polo positivo atraerá al polo negativo y viceversa, dando
como resultado una unión.
Las fuerzas intermoleculares que actúan entre las moléculas se clasifican en :
Dipolos permanentes
Este tipo de unión se produce cuando ambas moléculas disponen de cargas positivas y
negativas, es decir son moléculas polares o que tienen polaridad, atrayéndose electrostaticamente
y formando la unión.
Dipolos inducidos
Este tipo de unión se produce cuando una molécula no polar redistribuye la concentración de los
electrones (tiene la posibilidad de polarizarse) al acercarse una molécula polar, de tal forma que se
crea una unión entre ambas moléculas.
Dipolos dispersos
Este último caso la unión se produce entre moléculas no polares pero que pueden polarizarse,
y cuando esto último ocurren se atraen mutuamente creando la unión molecular.
Las fuerzas intermoleculares se definen como el conjunto de fuerzas atractivas y repulsivas
que se producen entre las moléculas como consecuencia de la presencia o ausencia de electrones.
Cuando dos o más átomos se unen mediante un enlace químico forman una molécula, los electrones
que conforman la nueva molécula recorren y se concentran en la zona del átomo con mayor
electronegatividad, definimos la electronegatividad como la propiedad que tienen los átomos
en atraer electrones.
La concentración de electrones en una zona específica de la molécula crea una carga negativa,
mientras que la ausencia de los electrones crea una carga positiva.
Denominamos dipolos a las moléculas que disponen de zonas cargadas negativamente y
positivamente debido a la electronegatividad y concentración de los electrones en las moléculas.
Podemos asimilar el funcionamiento de un dipolo a un imán con su polo positivo y su polo negativo,
de tal forma que si acercamos otro imán el polo positivo atraerá al polo negativo y viceversa, dando
como resultado una unión.
Las fuerzas intermoleculares que actúan entre las moléculas se clasifican en :
- Dipolos permanentes
- Dipolos inducidos
- Dipolos dispersos
Dipolos permanentes
Este tipo de unión se produce cuando ambas moléculas disponen de cargas positivas y
negativas, es decir son moléculas polares o que tienen polaridad, atrayéndose electrostaticamente
y formando la unión.
Dipolos inducidos
Este tipo de unión se produce cuando una molécula no polar redistribuye la concentración de los
electrones (tiene la posibilidad de polarizarse) al acercarse una molécula polar, de tal forma que se
crea una unión entre ambas moléculas.
Dipolos dispersos
Este último caso la unión se produce entre moléculas no polares pero que pueden polarizarse,
y cuando esto último ocurren se atraen mutuamente creando la unión molecular.
5.10 Características de los compuestos que se presentan un puente de hidrogeno, especialmente la del agua y las moléculas de importancia biológica
PROPIEDADES:
1. FÍSICAS
El agua es un líquido inodoro e insípido. Tiene un cierto color azul cuando se concentra en
grandes masas. A la presión atmosférica (760 mm de mercurio), el punto de fusión del agua
pura es de 0ºC y el punto de ebullición es de 100ºC, cristaliza en el sistema hexagonal, llamándose
nieve o hielo según se presente de forma esponjosa o compacta, se expande al congelarse, es decir
aumenta de volumen, de ahí que la densidad del hielo sea menor que la del agua y por ello el hielo flota
en el agua líquida. El agua alcanza su densidad máxima a una temperatura de 4ºC,que es de 1g/cc.
Su capacidad calorífica es superior a la de cualquier otro líquido o sólido, siendo su calor
específico de 1 cal/g, esto significa que una masa de agua puede absorber o desprender grandes
cantidades de calor, sin experimentar apenas cambios de temperatura, lo que tiene gran influencia en
el clima (las grandes masas de agua de los océanos tardan más tiempo en calentarse y enfriarse que
el suelo terrestre). Sus calores latentes de vaporización y de fusión (540 y 80 cal/g, respectivamente)
son también excepcionalmente elevados.
2. QUÍMICAS
El agua es el compuesto químico más familiar para nosotros, el más abundante y el de
mayor significación para nuestra vida. Su excepcional importancia, desde el punto de vista químico,
reside en que casi la totalidad de los procesos químicos que ocurren en la naturaleza, no solo en
organismos vivos, sino también en la superficie no organizada de la tierra, así como los que se llevan
a cabo en el laboratorio y en la industria, tienen lugar entre sustancias disueltas en agua, esto es en
disolución. Normalmente se dice que el agua es el disolvente universal, puesto que todas las sustancias
son de alguna manera solubles en ella.
No posee propiedades ácidas ni básicas, combina con ciertas sales para
formar hidratos, reacciona con los óxidos de metales formando ácidos y actúa
como catalizador en muchas reacciones químicas.
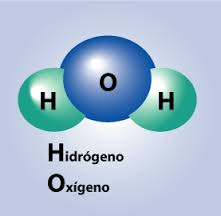
Características de la molécula de agua:
La molécula de agua libre y aislada, formada por un átomo de Oxigeno unido a otros dos átomos
de Hidrogeno es triangular. El ángulo de los dos enlaces (H-O-H) es de 104,5º y la distancia de
enlace O-H es de 0,96 A. Puede considerarse que el enlace en la molécula es covalente, con una
cierta participación del enlace iónico debido a la diferencia de electronegatividad entre los átomos
que la forman.
La atracción entre las moléculas de agua tiene la fuerza suficiente para producir un agrupamiento
de moléculas. La fuerza de atracción entre el hidrógeno de una molécula con el oxígeno de otra es
de tal magnitud que se puede incluir en los denominados enlaces de PUENTE DE HIDRÓGENO.
Estos enlaces son los que dan lugar al aumento de volumen del agua sólida y a las estructuras
hexagonales de que se habló más arriba.
IMPORTANCIA DE LAS MOLECULAS BIOLOGICAS ORGANICAS SENCILLAS
A diferencia de la composición química de la corteza terrestre, la composición de una
célula viva se fundamenta en un restringido conjunto de elementos, cuyos cuatro elementos
son: el carbono C, el hidrogeno H, el oxigeno O, y el nitrógeno N, y la suma de estos elementos
constituye el 99 % de su peso, esto ha traído como consecuencia, la aparición de una química de
la vida distinta a la química inorgánica, la química orgánica.
La sustancia más abundante en la célula es el agua que constituye el 70 % del peso de la célula..
Existen cuatro grandes familias de moléculas orgánicas pequeñas:
PROPIEDADES:
1. FÍSICAS
El agua es un líquido inodoro e insípido. Tiene un cierto color azul cuando se concentra en
grandes masas. A la presión atmosférica (760 mm de mercurio), el punto de fusión del agua
pura es de 0ºC y el punto de ebullición es de 100ºC, cristaliza en el sistema hexagonal, llamándose
nieve o hielo según se presente de forma esponjosa o compacta, se expande al congelarse, es decir
aumenta de volumen, de ahí que la densidad del hielo sea menor que la del agua y por ello el hielo flota
en el agua líquida. El agua alcanza su densidad máxima a una temperatura de 4ºC,que es de 1g/cc.
Su capacidad calorífica es superior a la de cualquier otro líquido o sólido, siendo su calor
específico de 1 cal/g, esto significa que una masa de agua puede absorber o desprender grandes
cantidades de calor, sin experimentar apenas cambios de temperatura, lo que tiene gran influencia en
el clima (las grandes masas de agua de los océanos tardan más tiempo en calentarse y enfriarse que
el suelo terrestre). Sus calores latentes de vaporización y de fusión (540 y 80 cal/g, respectivamente)
son también excepcionalmente elevados.
2. QUÍMICAS
El agua es el compuesto químico más familiar para nosotros, el más abundante y el de
mayor significación para nuestra vida. Su excepcional importancia, desde el punto de vista químico,
reside en que casi la totalidad de los procesos químicos que ocurren en la naturaleza, no solo en
organismos vivos, sino también en la superficie no organizada de la tierra, así como los que se llevan
a cabo en el laboratorio y en la industria, tienen lugar entre sustancias disueltas en agua, esto es en
disolución. Normalmente se dice que el agua es el disolvente universal, puesto que todas las sustancias
son de alguna manera solubles en ella.
No posee propiedades ácidas ni básicas, combina con ciertas sales para
formar hidratos, reacciona con los óxidos de metales formando ácidos y actúa
como catalizador en muchas reacciones químicas.
Características de la molécula de agua:
La molécula de agua libre y aislada, formada por un átomo de Oxigeno unido a otros dos átomos
de Hidrogeno es triangular. El ángulo de los dos enlaces (H-O-H) es de 104,5º y la distancia de
enlace O-H es de 0,96 A. Puede considerarse que el enlace en la molécula es covalente, con una
cierta participación del enlace iónico debido a la diferencia de electronegatividad entre los átomos
que la forman.
La atracción entre las moléculas de agua tiene la fuerza suficiente para producir un agrupamiento
de moléculas. La fuerza de atracción entre el hidrógeno de una molécula con el oxígeno de otra es
de tal magnitud que se puede incluir en los denominados enlaces de PUENTE DE HIDRÓGENO.
Estos enlaces son los que dan lugar al aumento de volumen del agua sólida y a las estructuras
hexagonales de que se habló más arriba.
IMPORTANCIA DE LAS MOLECULAS BIOLOGICAS ORGANICAS SENCILLAS
A diferencia de la composición química de la corteza terrestre, la composición de una
célula viva se fundamenta en un restringido conjunto de elementos, cuyos cuatro elementos
son: el carbono C, el hidrogeno H, el oxigeno O, y el nitrógeno N, y la suma de estos elementos
constituye el 99 % de su peso, esto ha traído como consecuencia, la aparición de una química de
la vida distinta a la química inorgánica, la química orgánica.
La sustancia más abundante en la célula es el agua que constituye el 70 % del peso de la célula..
Existen cuatro grandes familias de moléculas orgánicas pequeñas:
- Glúcidos o carbohidratos
- Lípidos
- Aminoácidos
- Ácidos nucleicos o Nucleótidos