Tabla Periódica
4.1 Antecedentes históricos de la clasificación de los elementos químicos
Durante los primeros 25 años del siglo XIX, se descubrieron unos 20 nuevos elementos. A
medida que el numero de elementos conocidos aumentaba resultaron evidentes las
semejanzas físicas y químicas entre algunos de ellos. Entonces los químicos
entendieron que el estudio de las propiedades de los elementos químicos era mas
fácil agrupándolos según sus propiedades semejantes en base a una ley
natural.
En busca de esta ley natural muchos químicos lograron ordenar los elementos, pero
recién en 1913 Henry Moseley descubrió el principio o ley natural
que guia la clasificación moderna: las propiedades de los elementos son funciones
periódicas de sus números atómicos.
El descubrimiento de esta ley periódica, necesitó dos acontecimientos previos:
·El establecimiento de una serie de pesos atómicos consistentes y dignos de
confianza.
·La concepción del átomo nuclear con un numero definido de protones e igual numero
de electrones que giran a su alrededor.
Las Triadas de Johan Dobereiner (1817)
El químico alemán Johan Dobereiner (1780 - 1849) agrupa
los elementos hasta entonces conocidos en serie de tres elementos
llamándolo “triadas”. Los elementos que pertenecen a una
triada poseen propiedades químicas semejantes. Además el elemento central posee
un peso atómico (P.A.) aproximadamente igual a la semisuma de los P.A. de los
elementos extremos.
Hacia 1850, los químicos habían llegado a identificar unas veinte triadas, Se descartó
de esta forma agruparlos, porque se descubrieron nuevos elementos que no
cumplían con las triadas.
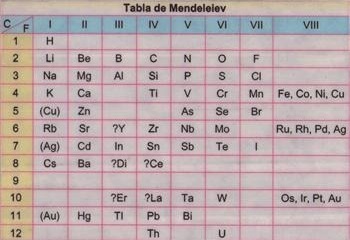
Tabla Periodica de Dimitri Mendeleiev y Lothar Meyer (1869)
Se denomina tabla periodica porque el ordenamiento esta basado en la variación
periódica de las propiedades de los elementos.
Descripción de la Tabla de Mendeleiev:
1. Los 63 elementos conocidos hasta ese entonces fueron ordenados en funcion
creciente a su peso atómico, en series (filas) y grupos (columnas).
2. Asigna a los elementos de un mismo grupo una valencia; así los elementos del
grupo III tendrán valencia igual a tres, por lo tanto el numero de grupo era
igual a la valencia.
3. Los elementos de un mismo grupo poseen propiedades semejantes, así por ejemplo
forman óxidos e hidruros de formulas similares porque tenían igual
valencia.
4. La tabla posee ocho grupos.
Durante los primeros 25 años del siglo XIX, se descubrieron unos 20 nuevos elementos. A
medida que el numero de elementos conocidos aumentaba resultaron evidentes las
semejanzas físicas y químicas entre algunos de ellos. Entonces los químicos
entendieron que el estudio de las propiedades de los elementos químicos era mas
fácil agrupándolos según sus propiedades semejantes en base a una ley
natural.
En busca de esta ley natural muchos químicos lograron ordenar los elementos, pero
recién en 1913 Henry Moseley descubrió el principio o ley natural
que guia la clasificación moderna: las propiedades de los elementos son funciones
periódicas de sus números atómicos.
El descubrimiento de esta ley periódica, necesitó dos acontecimientos previos:
·El establecimiento de una serie de pesos atómicos consistentes y dignos de
confianza.
·La concepción del átomo nuclear con un numero definido de protones e igual numero
de electrones que giran a su alrededor.
Las Triadas de Johan Dobereiner (1817)
El químico alemán Johan Dobereiner (1780 - 1849) agrupa
los elementos hasta entonces conocidos en serie de tres elementos
llamándolo “triadas”. Los elementos que pertenecen a una
triada poseen propiedades químicas semejantes. Además el elemento central posee
un peso atómico (P.A.) aproximadamente igual a la semisuma de los P.A. de los
elementos extremos.
Hacia 1850, los químicos habían llegado a identificar unas veinte triadas, Se descartó
de esta forma agruparlos, porque se descubrieron nuevos elementos que no
cumplían con las triadas.
Tabla Periodica de Dimitri Mendeleiev y Lothar Meyer (1869)
Se denomina tabla periodica porque el ordenamiento esta basado en la variación
periódica de las propiedades de los elementos.
Descripción de la Tabla de Mendeleiev:
1. Los 63 elementos conocidos hasta ese entonces fueron ordenados en funcion
creciente a su peso atómico, en series (filas) y grupos (columnas).
2. Asigna a los elementos de un mismo grupo una valencia; así los elementos del
grupo III tendrán valencia igual a tres, por lo tanto el numero de grupo era
igual a la valencia.
3. Los elementos de un mismo grupo poseen propiedades semejantes, así por ejemplo
forman óxidos e hidruros de formulas similares porque tenían igual
valencia.
4. La tabla posee ocho grupos.
Ventajas de esta Tabla:
1. Permitió tener una visión mas general de la clasificación periódica de los
elementos ordenados por grupos y periodos.
2. Al dejar ciertos casilleros vacíos, predijo la existencia de nuevos elementos y
sus propiedades físicas y químicas. Por ejemplo en el grupo III y IV, predijo la
existencia del Escandio, Galio, Germanio, etc.
Desventajas de la Tabla:
1. Los metales y no metales no se encuentran bien diferenciados.
2. Se asigna valencia única para cada elemento, actualmente se sabe que algunos
elementos tienen mas de una valencia.
3. Ciertos elementos no cumplían el orden creciente del peso atómico, por lo que
Mendeleiev permutó arbitrariamente algunos elementos de un grupo a otro.
1. Permitió tener una visión mas general de la clasificación periódica de los
elementos ordenados por grupos y periodos.
2. Al dejar ciertos casilleros vacíos, predijo la existencia de nuevos elementos y
sus propiedades físicas y químicas. Por ejemplo en el grupo III y IV, predijo la
existencia del Escandio, Galio, Germanio, etc.
Desventajas de la Tabla:
1. Los metales y no metales no se encuentran bien diferenciados.
2. Se asigna valencia única para cada elemento, actualmente se sabe que algunos
elementos tienen mas de una valencia.
3. Ciertos elementos no cumplían el orden creciente del peso atómico, por lo que
Mendeleiev permutó arbitrariamente algunos elementos de un grupo a otro.
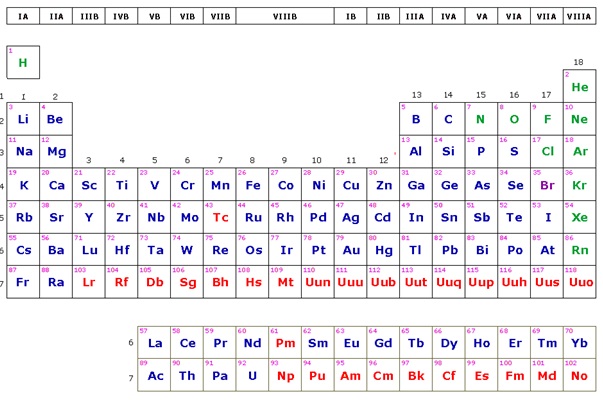
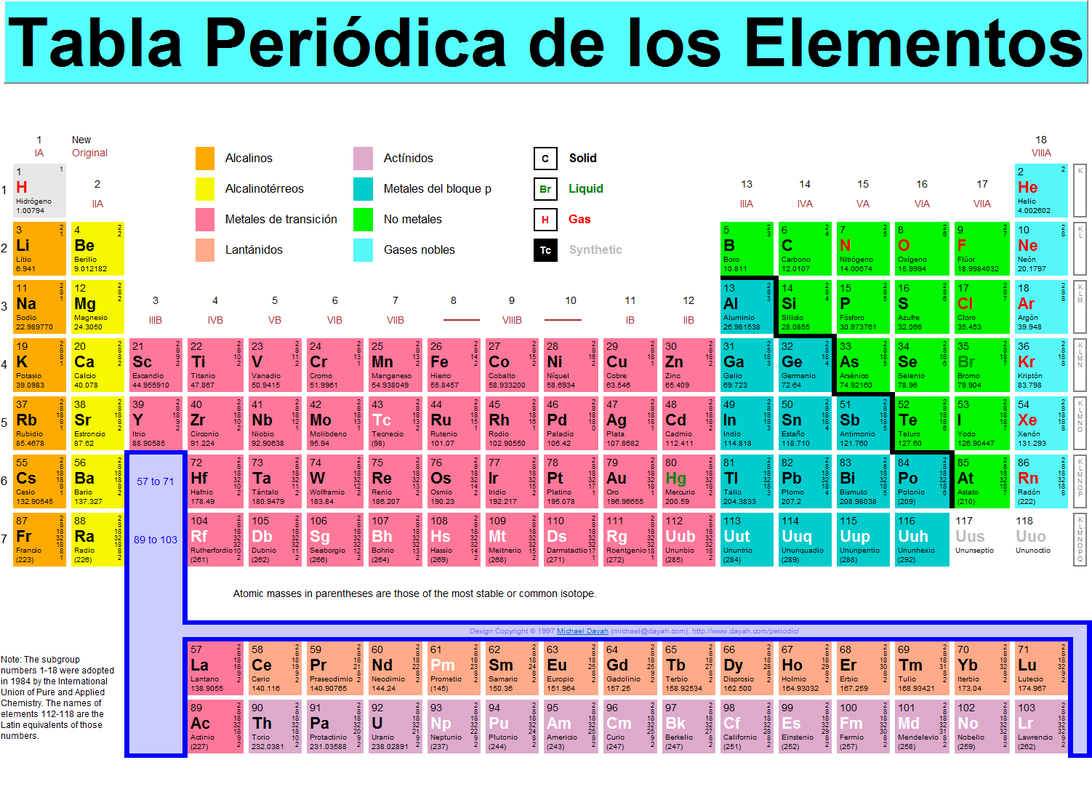
4.2 Grupo, periodo y bloque
Periodos
Son los renglones o filas horizontales de la tabla periódica. Actualmente se
incluyen 7 periodos en la tabla periódica.
Grupos
Son las columnas o filas verticales de la tabla periódica. La tabla periódica consta
de 18 grupos. Éstos se designan con el número progresivo, pero está muy
difundido el designarlos como grupos A y grupos B númerados con con números
romanos. Las dos formas de designarlos se señalan en la tabla periódica mostrada
al inicio del tema.
Clases: Se distinguen 4 clases en la tabla periódica
Elementos Representativos: Están formados por los elementos de los grupos "A".
Elementos De Transición: Elementos de los grupos "B", excepto lantánidos y actínidos.
Elementos De Transición Interna: Lantánidos y actínidos.
Gases Nobles: Elementos del grupo VIII A (18)
Periodos
Son los renglones o filas horizontales de la tabla periódica. Actualmente se
incluyen 7 periodos en la tabla periódica.
Grupos
Son las columnas o filas verticales de la tabla periódica. La tabla periódica consta
de 18 grupos. Éstos se designan con el número progresivo, pero está muy
difundido el designarlos como grupos A y grupos B númerados con con números
romanos. Las dos formas de designarlos se señalan en la tabla periódica mostrada
al inicio del tema.
Clases: Se distinguen 4 clases en la tabla periódica
Elementos Representativos: Están formados por los elementos de los grupos "A".
Elementos De Transición: Elementos de los grupos "B", excepto lantánidos y actínidos.
Elementos De Transición Interna: Lantánidos y actínidos.
Gases Nobles: Elementos del grupo VIII A (18)
4.3 Propiedades periódicas (electronegatividad, energía de ionización, afinidad electrónica, radio y volumen atómico) y su variación en la tabla periódica.
Las propiedades periódicas
Son propiedades que presentan los átomos de un elemento y que varían en la Tabla
Periódica siguiendo la periodicidad de los grupos y periodos de ésta. Por la posición de
un elemento podemos predecir qué valores tendrán dichas propiedades así como a través
de ellas, el comportamiento químico del elemento en cuestión. Tal y como hemos dicho, vamos
a encontrar una periodicidad de esas propiedades en la tabla. Esto supone por ejemplo, que la
variación de una de ellas en los grupos o periodos va a responder a una regla general. El conocer
estas reglas de variación nos va a permitir conocer el comportamiento, desde un punto de vista químico,
de un elemento, ya que dicho comportamiento, depende en gran manera de sus propiedades periódicas.
Propiedades más importantes
Hay un gran número de propiedades periódicas. Entre las más importantes destacaríamos:
- Estructura electrónica
- Radio atómico
- Volumen atómico
- Potencial de ionización
- Afinidad electrónica
- Electronegatividad:
- Carácter metálico
- Valencia iónica
- Valencia covalente
- Radio iónico
- Radio covalente
Y también las siguientes propiedades físicas tienen una variación periódica:
- Densidad
- calor específico
- Punto de ebullición
- Punto de fusión
Las propiedades periódicas
Son propiedades que presentan los átomos de un elemento y que varían en la Tabla
Periódica siguiendo la periodicidad de los grupos y periodos de ésta. Por la posición de
un elemento podemos predecir qué valores tendrán dichas propiedades así como a través
de ellas, el comportamiento químico del elemento en cuestión. Tal y como hemos dicho, vamos
a encontrar una periodicidad de esas propiedades en la tabla. Esto supone por ejemplo, que la
variación de una de ellas en los grupos o periodos va a responder a una regla general. El conocer
estas reglas de variación nos va a permitir conocer el comportamiento, desde un punto de vista químico,
de un elemento, ya que dicho comportamiento, depende en gran manera de sus propiedades periódicas.
Propiedades más importantes
Hay un gran número de propiedades periódicas. Entre las más importantes destacaríamos:
- Estructura electrónica
- Radio atómico
- Volumen atómico
- Potencial de ionización
- Afinidad electrónica
- Electronegatividad:
- Carácter metálico
- Valencia iónica
- Valencia covalente
- Radio iónico
- Radio covalente
Y también las siguientes propiedades físicas tienen una variación periódica:
- Densidad
- calor específico
- Punto de ebullición
- Punto de fusión
4.4 Utilidad e importancia de los metales y no metales para la vida socioeconómica del país.
Todas las personas deberíamos saber la importancia que tiene los Elementos Metales y
No Metales para los seres vivos, ya que algunos son fundamentales para la vida.
Dichos elementos, especialmente algunos no metales son los más importantes de la
vida de los seres vivos algunos de estos elementos son el oxigeno y el hidrógeno que
se encuentran en la atmósfera y en el agua haciéndolos sumamente importantes para la vida.
Los Metales también son importantes, pero no tanto. Estos son mas que todo utilizados
en industrias, construcción de casa, y de adornos o joyas.
Elementos metales, y no metales
Son elementos químicos con altos puntos de fusión y de ebullición; son
indispensables y los podemos encontrar en todas partes. Se utilizan en el hogar
y en algunos trabajos.
Propiedades Físicas
Brillo: reflejan la luz que incide en su superficie.
Dureza: la superficie de los metales oponen resistencia e dejarse rayar por objetos agudos.
Tenacidad: los elementos presentan mayor o menor resistencia a romperse cuando ejercen
sobre ellos una presión.
Ductibilidad: los metales son fácilmente estirados en hilos finos(alambres), sin romperse.
Maleabilidad: ciertos metales, tales como el oro, la plata y el cobre, presentan la propiedad
de ser reducidos a delgadas láminas, sin romperse.
Conductividad Calórica: los metales absorben y conducen la energía calórica.
Conductividad Eléctrica: los metales permiten el paso de la corriente eléctrica a través de su masa.
Densidad: la inmensa mayoría de los metales presentan altas densidades.
Fusibilidad: la inmensa mayoría de los metales presentan elevadísimos puntos de fusión, en mayor
o menor medida para ser fundidos.
Propiedades Químicas
Reaccionan con los ácidos para formar sales.
Forman iones electropositivos o cationes.
Reaccionan con el oxigeno para formar óxidos básicos.
Forman aleaciones.
Algunos metales químicamente más activos desplazan a otros de sus compuestos.
Estado Natural:
La inmensa mayoría de los metales que conocemos se encuentran en la naturaleza
formado compuestos, tales como: óxidos, silicatos, carbonatos, sulfatos y
sulfuros. Sin embargo, existen un numero escaso de elementos, como el oro, la
plata y el platino, que se pueden hallar libres, es decir, no
combinados.
Todas las personas deberíamos saber la importancia que tiene los Elementos Metales y
No Metales para los seres vivos, ya que algunos son fundamentales para la vida.
Dichos elementos, especialmente algunos no metales son los más importantes de la
vida de los seres vivos algunos de estos elementos son el oxigeno y el hidrógeno que
se encuentran en la atmósfera y en el agua haciéndolos sumamente importantes para la vida.
Los Metales también son importantes, pero no tanto. Estos son mas que todo utilizados
en industrias, construcción de casa, y de adornos o joyas.
Elementos metales, y no metales
Son elementos químicos con altos puntos de fusión y de ebullición; son
indispensables y los podemos encontrar en todas partes. Se utilizan en el hogar
y en algunos trabajos.
Propiedades Físicas
Brillo: reflejan la luz que incide en su superficie.
Dureza: la superficie de los metales oponen resistencia e dejarse rayar por objetos agudos.
Tenacidad: los elementos presentan mayor o menor resistencia a romperse cuando ejercen
sobre ellos una presión.
Ductibilidad: los metales son fácilmente estirados en hilos finos(alambres), sin romperse.
Maleabilidad: ciertos metales, tales como el oro, la plata y el cobre, presentan la propiedad
de ser reducidos a delgadas láminas, sin romperse.
Conductividad Calórica: los metales absorben y conducen la energía calórica.
Conductividad Eléctrica: los metales permiten el paso de la corriente eléctrica a través de su masa.
Densidad: la inmensa mayoría de los metales presentan altas densidades.
Fusibilidad: la inmensa mayoría de los metales presentan elevadísimos puntos de fusión, en mayor
o menor medida para ser fundidos.
Propiedades Químicas
Reaccionan con los ácidos para formar sales.
Forman iones electropositivos o cationes.
Reaccionan con el oxigeno para formar óxidos básicos.
Forman aleaciones.
Algunos metales químicamente más activos desplazan a otros de sus compuestos.
Estado Natural:
La inmensa mayoría de los metales que conocemos se encuentran en la naturaleza
formado compuestos, tales como: óxidos, silicatos, carbonatos, sulfatos y
sulfuros. Sin embargo, existen un numero escaso de elementos, como el oro, la
plata y el platino, que se pueden hallar libres, es decir, no
combinados.